Plein d’informations utiles dans différents domaines
Informatique pratique
Cours pour les petits et les grands (de la maternelle à la fac)
Anesthésie
Préop
Consultation / Examens préopératoire / ECBU préop
Évaluation cardiovasculaire en chirurgie non cardiaque / ECG
Intubation difficile ? Ventilation au masque difficile ? Risque allergique / Risque d’inhalation (Jeûne préopératoire)
Prémédication / Adaptation des traitements (Corticothérapie / antiépileptique / AVK / béta bloquants)
Coronariens
Pacemaker (cardioverteur/défibrillateur) et anesthésie
CMO …
Valvulopathies
Anesthésie pour craniotomie, pour chirurgie transphénoïdale.
Anesthésie du paraplégique
Anesthésie et sismothérapie
Maladie de Parkinson, myasthénie, porphyries, Qt long, Sd de Brugada
Sd de WPW
Anesthésie et maladies rares, et estomac plein, et diabète, cirrhotique, VIH+, Obèse, SAOS
EFR, Anesthésie pour chirurgie pulmonaire, HTAP
Transplantation rénale, hépatique
Tumeur carcinoïde, Phéochromocytomes, autres tumeurs surrénaliennes
Œdème angioneurotique héréditaire
Mastocytoses systémiques
Chimiothérapie et anesthésie
Anesthésie et dépendance aux opiacés, et pathologie psychiatrique et sujet âgé
Réhabilitation précoce postopératoire
Stratégie (d’épargne) transfusionnelle et anémie péri-opératoire / Acide tranexamique
Antiplaquettaire / Prévention du risque thrombotique veineux en chirurgie / Utilisation des AVK / Utilisation des ADO
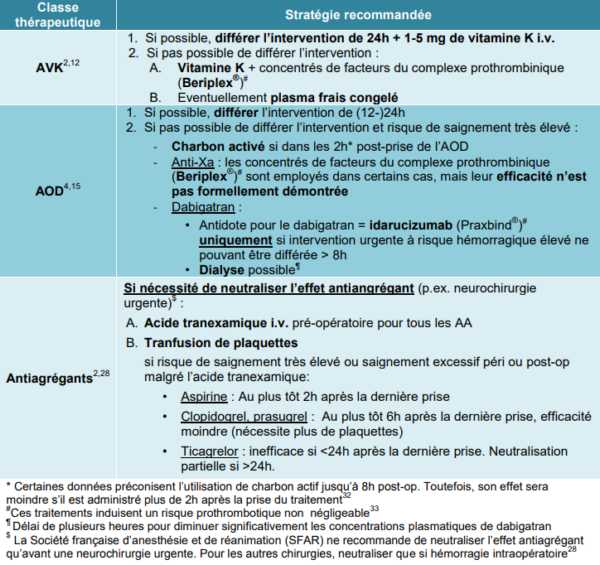
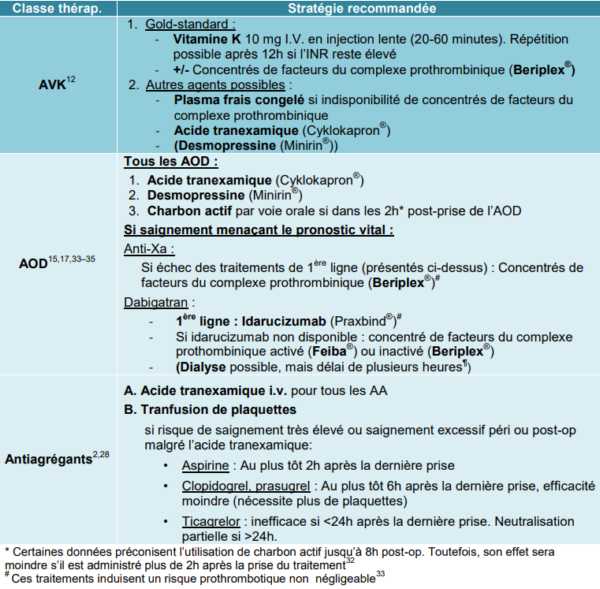
Antagonisation des AVK, des héparines et des ADO
TIH, hémophilie, Maladie de Willebrand
TT, TCA, TQ
Troubles biologiques rencontrés dans les Sd hémorragiques les plus fréquents
Chez l'enfant
Chez l'adulte
Évaluation du risque cardiaque en chirurgie non cardiaque
Mêmes les chirurgie non cardiaque peuvent être une cause de morbidité et de mortalité.
D’où la nécessité d’une stratification du risque cardiovasculaire, selon des facteurs liés au patient (cardiopathies actives, facteurs de risque clinique, capacité fonctionnelle) et à la chirurgie prévue.
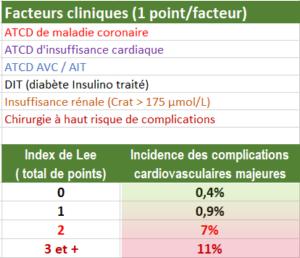
Risque cardiaque lié au terrain (score de Lee)
Une évaluation cardiologique préopératoire est requise pour les patients à haut risque de complications
Risque cardiaque lié à la chirurgie
< 1% d’événements cardiovasculaires
– Endoscopie, ambulatoire
– Chirurgie superficielle, mammaire, ophtalmo, dentaire
– Endocrinienne : thyroïde
– Reconstructrice
– Carotidienne asymptomatique (EnCa ou StCa)
– Gynécologique mineure
– Orthopédique mineure (méniscectomie)
– Urologique mineure (résection transurétrale de la prostate)
– Intrapéritonéale : splénectomie, hernie hiatale, cholécystectomie
– Carotidien symptomatique
– Angioplastie artérielle périphérique
– Anévrisme voie endovasculaire
– Chirurgie cervico-faciale, Neurochirurgie ou
orthopédique : majeure (chirurgie de la hanche et la
colonne vertébrale)
– Urologiques ou gynécologiques
– transplantation rénale
– Chirurgie thoracique majeure
– Chirurgie aortique et vasculaire majeure
– Revascularisation de membre inférieure ou amputation ou thrombo embolectomie
– Chirurgie Duodénopancréatique
– Résection hépatique, chirurgie canal biliaire
– Oesophagectomie
– Réparation de perforation de l’intestin
– Résection surrénalienne
– Cystectomie totale
– Pneumonectomie, Greffe pulmonaire ou une
greffe du foie
? Fleisher LA, Circulation 2007
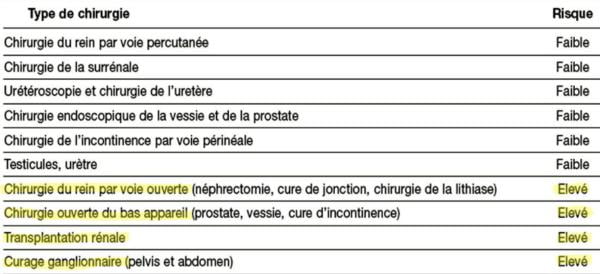
Risque hémorragique / thrombotique
Classification des risques hémorragiques
= actes responsables de saignements peu fréquents, de faible intensité ou aisément contrôlés, pouvant être réalisés chez des patients anticoagulés à taux thérapeutiques.
Chirurgie cutanée, de la cataracte, certains actes de rhumatologie à faible risque hémorragique, certains actes de chirurgie bucco-‐dentaire, certains actes d’endoscopie digestive (liste non limitative).
Neurochirurgie intracrânienne ou les PL /Rachi anesthésies
Rivaroxaban 15mg x2 pendant 3 semaines
(Apixaban 10mg x2 pendant 10j)
==> éviter de programmer une chirurgie
Pas de relais pas de dosages (si délais d’arrêt respectés)
Reprise à dose préventive après 6h (HBPM ?)
Anticoagulation à dose « curative » dès que l’hémostase le permet (entre 24 et 72 heures).
Pas de chevauchement des molécules, attendre 12h après l’HBPM
Classification de la nécessité de l'anticoagulation selon le patient
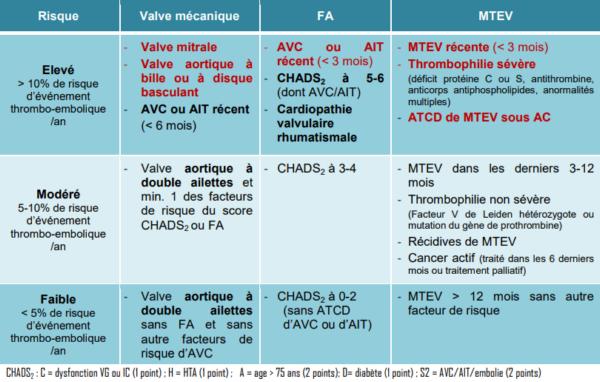
Classification des risques thrombotiques selon le patient
- Les ATCD d’évènement thrombo-embolique veineux
- La thrombophilie familiale majeure
- Le cancer
- La chimiothérapie
- L’insuffisance cardiaque ou respiratoire
- L’hormonothérapie ,La contraception orale
- Les AVC avec déficit neurologique
- Le postpartum
- L’âge et l’obésité
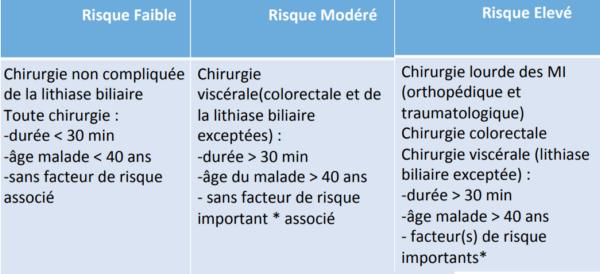
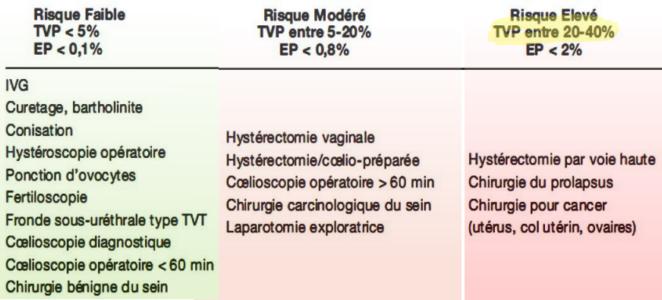
Classification des risques thrombotiques par chirurgie
• chirurgie orthopédique et traumatologique:
• La chirurgie digestive
• chirurgie urologique
• chirurgie gynécologique
• Après césarienne ,post partum
• Thoracique et cardiovasculaire
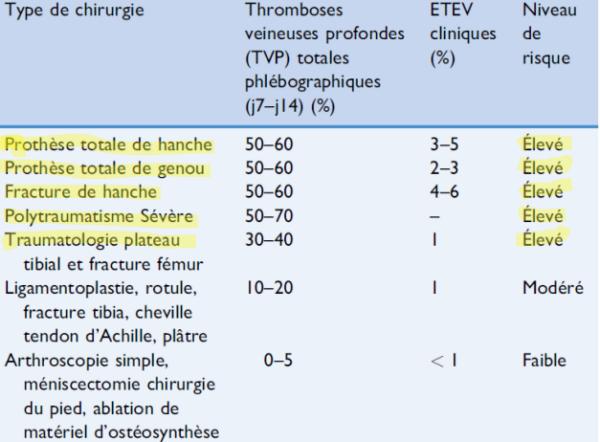
Quelques chiffres pour certaines chirurgies
FA et anticoagulation selon P. TABOULET
(site E-cardiogram.com)
Les anticoagulants peuvent être utiles pour réduire le risque thromboembolique (TE) associé à une fibrillation ou un flutter atrial [1] .
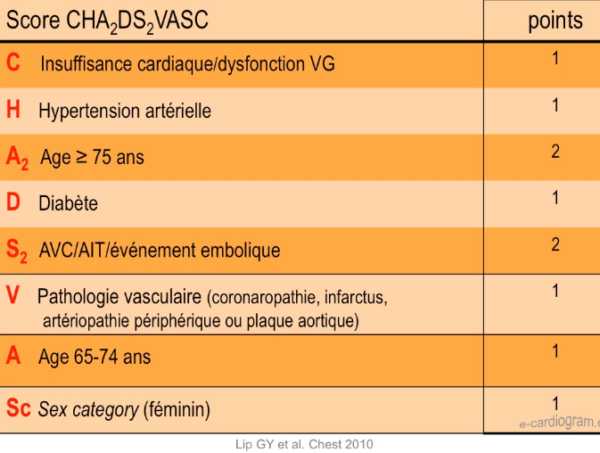
- Le risque estimé selon le score CHA2DS2-VASc varie de 0 à 9 points et prédit une incidence annuelle d’AVC variable entre < 1 % et > 20 % (respectivement 0,8 ; 2,0 ; 3,7 ; 5,9 ; 9,3 ; 15,3 ; 19,7 ; 21,5 ; 22,4 ; 23,6 %) [2]. Soit x2 jusque 4 puis x3 de 5 à 9 (environ)
- Il augmente pour une FA de durée > 48 heures et après cardioversion (entre le 3e et le 30e jour).
Tous les patients qui présentent une FA doivent avoir une estimation du risque thromboembolique (TE), quel que soit le rythme cardiaque au moment de l’examen (ex. conversion ou cardioversion). L’estimation du risque TE est essentielle à la prise en charge thérapeutique. Elle repose sur le score CHA2DS2-VASc (1). Pour simplifier, le risque TE la première année de découverte d’une FA est x 2 de 1 à 4 puis x 3 au delà.
- Les facteurs de haut risque d’accident thromboembolique sont : un âge supérieur à 75 ans, un antécédent d’accident vasculaire cérébral (AVC), accident ischémique transitoire (AIT) ou embolie systémique [1], un rétrécissement mitral ou la présence d’une prothèse valvulaire cardiaque mécanique [3].
- Un traitement anticoagulant au long court par anticoagulant oral est recommandé en présence d’un facteur de risque thrombo-embolique (grade 1A), à l’exception du sexe féminin.
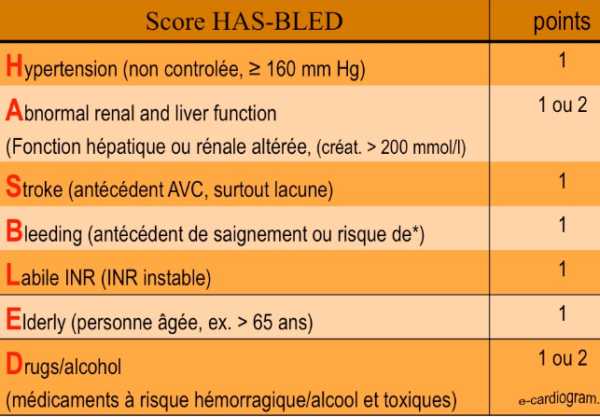
Tous les patients présentant une FA doivent avoir une évaluation formelle du risque hémorragique (ex. score HAS-BLED [1][4]).
- Chez les patients ayant un score HAS-BLED ≥ 3, prudence et examens réguliers sont appropriées, ainsi que les efforts à corriger les facteurs de risque potentiellement réversibles de saignement. Le HAS-BLED score ne doit pas être utilisé pour exclure les patients de la thérapie OAC, mais permettre aux cliniciens de faire une évaluation éclairée du risque hémorragique.
- Le risque hémorragique doit être mis en balance avec le bénéfice attendu par un traitement AVK bien suivi (réduction d’environ 60% de l’incidence annuelle d’embolie systémique), le bénéfice étant d’autant plus fort que le risque primaire est élevé. Si le score HAS-BLED est supérieur au score CHADS2, le risque hémorragique est supérieur au bénéfice potentiel d’une ACG orale (3). Un niveau élevé de score HAS-BLED, soit à partir de 3 (taux d’accident élevé).
La définition d’AIT désignait un déficit neurologique < 24 h, après 2002 la limite est passée à moins d’une heure puis on est passé à une définition tissulaire car l’évolution des techniques d’imagerie ont montré qu’environs 30% des patients atteints d’AIT ≤ 24 heures présentaient un accident ischémique constitué (AIC) sur l’imagerie cérébrale.
Actuellement l’AHA définit l’AIT comme tout déficit neurologique transitoire en rapport avec une ischémie cérébrale ou rétinienne sans nécrose tissulaire [1].
On avance aussi le terme de syndrome neurovasculaire aigu pour définir la situation clinique correspondant à un déficit neurologique focal d’installation brutale d’origine vasculaire présumée.
Le score ABCD…
a été développé pour estimer le risque d ’AVC dans la semaine qui suit l’AIT [3].
Il est coté sur 6 points à partir de quatre paramètres cliniques dont chacun est apparu prédictif d’AVC :
● A pour âge (1 point si âge ≥ 60 ans),
● B pour blood pressure (1 point si antécédents d’HTA définis par le recours à un traitement antihypertenseur ou si PAS > 140 mmHg ou PAD ≥ 90 mmHg),
● C pour clinical features (2 points si déficit moteur unilatéral, 1 point si dysarthrie ou aphasie sans déficit moteur, 0 point pour tout autre type de symptôme),
● et D pour duration of symptoms (2 points si durée des symptômes ≥ 60 minutes, 1 point si durée comprise entre 10 et 59 minutes, 0 point si durée < 10 minutes).
en rajoutant le diabète (nécessité d’un traitement antidiabétique), on obtient le score ABCD2 utilisé aujourd’hui qui est coté sur 7 points.
Ce score prédit le risque d’AVC dans les 48 heures qui suivent un AIT.
Le risque d’AVC à 48 heures est de :
● 0 % pour un score 0 ou 1,
● de 1,3 % pour un score 2 ou 3,
● de 4,1 % pour un score 4 ou 5,
● et de 8,1 % pour un score 6 ou 7,
permettant de classer les patients en groupes à risque faible (scores 0 à 3), intermédiaire (scores 4 et 5) ou élevé (scores 6 et 7).
L’AHA préconise d’hospitaliser tout AIT vu dans les 72 heures si ABCD2 ≥ 3 [1] ;
Pour le National Institute for Clinical Excellence (NICE) il faut hospitaliser si ABCD2 ≥ 4,
les autres patients devant bénéficier du bilan étiologique de l’AIT dans la semaine [5].
Références
1. EASTON JD, SAVER JL, ALBERS GW et al. Definition and evaluation of transient ischemic attack : a scientific statement for healthcare professionals. Stroke, 2009 ; 40 : 2 276-93.
2. GILES MF, ROTHWELL PM. Transient ischaemic attack : clinical relevance, risk prediction and urgency of secondary prevention. Curr Opin Neurol, 2009 ; 22 : 46-53.
3. ROTHWELL PM, GILES MF, FLOSSMANN E et al. A simple score (ABCD) to identify individuals at high early risk of stroke after transient ischaemic attack. Lancet, 2005 ; 366 : 29-36.
4. JOHNSTON SC, ROTHWELL PM, NGUYEN-HUYNH MN et al. Validation and refinement of scores to predict very early stroke risk after transient ischaemic attack. Lancet, 2007 ; 369 : 283-92.
5. AMARENCO P, LABREUCHE J, LAVALLEE PC et al. Does ABCD2 score below 4 allow more time to evaluate patients with a transient ischemic attack ? Stroke, 2009 ; 40 : 3 091-5.
Références
[1] Hindricks G, Potpara T, Dagres N, et al; ESC Scientific Document Group. 2020 ESC Guidelines for the diagnosis and management of atrial fibrillation developed in collaboration with the European Association of Cardio-Thoracic Surgery (EACTS). Eur Heart J. 2020 Aug 29:ehaa612. (free access) Lire aussi Camm AJ, Lip GY, 2012 focused update of the ESC Guidelines for the management of atrial fibrillation: An update of the 2010 ESC Guidelines for the management of atrial fibrillation. Eur Heart J. 2012;33:2719-47 (free access)
[2] Taboulet P, Duchenne J, Lefort H, et al. Prise en charge de la fibrillation atriale en médecine d’urgence. Recommandations de la SFMU en partenariat avec la SFC. Ann. Fr. Med. Urgence (2015)
[3] Singer DE, et al. American College of Chest Physicians. Antithrombotic therapy in atrial fibrillation: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines (8th Edition). Chest. 2008;133(6 Suppl):546S-592S.
[4] Pisters R et al. A novel user friendly score (HAS-BLED) to assess one-year risk of major bleeding in atrial fibrillation patients: The Euro Heart Survey. Chest. 2010;138(5):1093-100
Indications des anticoagulants
La décision d’anticoaguler un patient dépend de plusieurs facteurs [2] :
- La FA est-elle récente ≤ 48 h ?
- Une cardioversion doit-elle être réalisée ?
- Existe-t-il un facteur déclenchant précis ?
- Le patient a-t-il des facteurs de risque embolique CHA2DS2-VASc ou un rétrécissement mitrale ?
- Le patient a-t-il des facteurs de risque hémorragique (en particulier digestif, cérébral, urologique) ?
- Quelles sont les préférences du patient ?
- si crise réduite ≤ 48 h : rien (solution préférable) ou AOD quatre semaines, recommandé en médecine d’urgence [2]
- si crise non réduite > 48 h et pas de cardioversion programmée : rien [2]
- si crise non réduite > 48 h et cardioversion programmée : AOD ou AVK à dose efficace* avec INR (2,5) au moins trois semaines (ou une ETO qui élimine la présence d’une thrombose de l’auriculaire gauche) avant cardioversion et quatre semaines au delà. Une HBPM est acceptable.
L’aspirine n’a plus de place dans la prévention du risque TE induit par la FA
( » antiplatelet therapy cannot be recommended for stroke prevention in AF patients« ) [1]
- si crise réduite ≤ 48 h et absence de facteur déclenchant : un traitement par ACO est recommandé (niveau IIA) [2]. Chez une femme < 65 ans, sans autre facteur de risque, aucun traitement n’est recommandé.
- si crise réduite ≤ 48 h + facteur déclenchant identifié et corrigé : un traitement par ACO est discutable (discussion avec le patient et interdisciplinarité; un délai de réflexion est souvent nécessaire : dans l’intervalle de réflexion, on peut donner une HBPM ou rien)
- pas de cardioversion sans ETO. Si la cardioversion est spontanée la conduite à tenir est la même que ci-dessous :
- héparinothérapie efficace (HNF ou HBPM) jusqu’au relais ACO
- ACO efficace (AOD ou AVK INR 2,5) jusqu’à une éventuelle cardioversion programmée (cf. ci-dessus) sauf contrindication (voir score HAS-BLED).
si crise mal tolérée et cardioversion précoce avant 48 h (électrique ou pharmacologique) : une héparinothérapie efficace est recommandée, si possible au préalable (recommandation IC), suivie par une anticoagulation efficace au moins quatre semaines ou davantage si facteurs de risque.
- si AIT x = urgence anticoagulation
- Pas d’héparinothérapie préalable sauf éventuellement si AIT répétés et rapprochés.
Pas d’aspirine ou autre antiagrégant, même en cas de récidive d’AVC sous AVK efficace.
- un traitement antiplaquettaire par aspirine (à la posologie de 325 mg/j) est recommandé après un AVC ischémique en attendant la décision d’anticoaguler efficacement. Des doses ≥ 50 mg sont acceptables.
- Une prophylaxie de la maladie thrombo-embolique veineuse par une injection sous-cutanée d’anticoagulant est recommandée. IPP à envisager.
- Une ACO ne doit être envisagée qu’après un délai dépendant de la sévérité de l’AVC et une absence d’hémorragie cérébrale à ce stade
En l’absence d’évènement ischémique ou angioplastie/stent dans l’année précédente :
- AOD (ou AVK) en monothérapie et STOP antiplaquettaires
En présence d’évènement ischémique ou stent dans l’année précédente :
- Antithrombotic strategies following coronary artery stenting in patients with AF at moderate to high thrombo-embolic risk
Gestion des traitements anticoagulants (AVK, AOD, Anti plaquettaires)

Pas d’arrêt des traitements
En préop : pas de prise la veille et le matin de l’intervention (si 1 seule prise è pas de prise le jours de l’intervention uniquement), pas de relais pas de dosage.
Reprise à l’heure habituelle (à 6h de la fin de l’intervention)
J-3 ( si cl créat > ou = 30) à J-5 (entre 30 et 50)
J-4 si Cl. Créat > 50
Neurochirurgie intracrânienne ou les PL /Rachi anesthésies
Délais d’arrêt plus long (dernière prise à J-5) pour les xabans et le dabigatran (en l’absence d’insuff. Rénale) sans relais avec une héparine (± mesure [AOD] si accumulation suspectée (insuff. Rénale, > 80 ans)
Pas de PL ou de péri/rachi anesthésie ou de bloc profond si [AOD] > 0 délais d’arrêt insuffisant
Rivaroxaban 15mg x2 pendant 3 semaines
(Apixaban 10mg x2 pendant 10j)
==> éviter de programmer une chirurgie
Pas de relais pas de dosages (si délais d’arrêt respectés)
Reprise à dose préventive après 6h (HBPM ?)
Anticoagulation à dose « curative » dès que l’hémostase le permet (entre 24 et 72 heures).
Pas de chevauchement des molécules, attendre 12h après l’HBPM
Risque infectieux
Antibioprophylaxie
Adaptation des trt
Per op
Post op
Réanimation
Cardiologique
Respiratoire
Pression motrice = Pplat – PEEPtot (= ΔP) < 14 cmH2O
6 ml/kg de poids prédit
au repos les muscles respiratoires consomment moins de 5% de l’oxygène
Compliance = Vt / ΔP en moyenne = 50ml/cmH2O chez l’adulte
PEP élevé > 14 cmH2O (augmenter PEP jusqu’à Pplateau <29
On calcul le Pa/Fi en PEP 5 et Vt = 6 ml/kg PP
Manœuvre de recrutement (= dangereux à utiliser avec prudence)
Légionellose => lévofloxacine (FQ)

(Calculateur poids idéal selon la taille)
(Calculateur BMI)

Algorithme de prise en charge des SDRA selon la gravité en utilisant le Pa/Fi
Calculateur Pa/Fi
SDRA léger
VNI possible
(ne doit pas retarder une intubation)
Ventilation protectrice (6 ml/kg PP)
PEP basse / modérée (5 à 10)
(Pa/Fi = 300 à 150)
SDRA modéré
Ventilation protectrice (6 ml/kg PP)
PEP moyenne / PEP élevée > 14 cm H2O
(SDRA MODÉRE SÉVÈRE)
CURARISATION (Pa/Fi < 150)
SDRA sévère
Ventilation protectrice (6 ml/kg PP)
PEP élevée > 14 cm H2O
CURARISATION
(dès que le Pa/Fi < 150)
Décubitus ventral
HFO (abandonné le 22 janvier 2013)
ECMO
Hydro Electrolytique
Rénale
Évaluation de la fonction rénale
Infectieuse
Vous pouvez nous contacter à l’adresse contact@pratiquement.com